公司注重生物药的创新性研发,产品管线丰富,包括单抗,双抗,单域抗体等多种抗体类型,适应症主要聚焦于肿瘤和自身免疫性疾病领域,研发靶点涵盖了PD-L1、EGFR、CD47、CSF-1R、CLDN18.2 等免疫检查点,包含了肿瘤微环境的各种方面的因素。现阶段公司有9个在研产品,其中4个已处在临床研究阶段,截至目前公司已获得7个临床批件。
项目
靶点
分子形式
适应症
Discovery
Pre-clinical
IND
Phase I
Phase II
Phase III
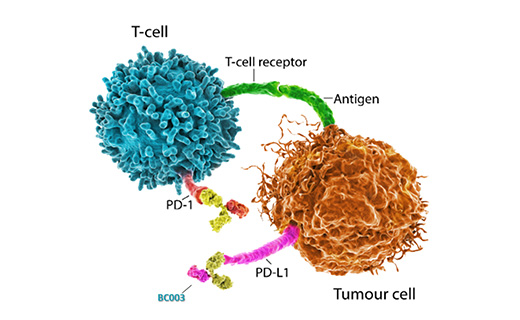
全人源IgG1抗PD-L1单克隆抗体,野生型Fc,有ADCC效应
临床 II 期单药治疗晚期非透明细胞肾癌临床正在进行中
临床 I 期单药治疗复发或转移性鼻咽癌正在进行中:安全性良好,初步有效性: ORR=26.7% (4/15)
BC003联合BC001用于治疗晚期实体瘤的Ia期临床试验正在进行
BC003多个联合用药的临床正在计划
重组抗EGFR人鼠嵌合型IgG1单克隆抗体, CDR区序列与西妥昔一致
Ia期单药以“3+3“方式完成了400、500、750mg/m2 3个剂量组爬坡,结果显示安全可耐受
Ib期临床联合化疗(TIP)治疗晚期阴茎癌:安全性可控,未观察到新的安全性信号; 初步有效性: ORR=94.1% (16/17); 关键性临床研究正在计划中
BC001联合BC003用于治疗晚期实体瘤的Ia期临床试验正在进行中
国内首个CSF-1R单抗
全人源IgG1单抗 ,具有ADCC功能
探索性临床 I 期正在进行中
进一步可开发的适应症包含:腱鞘巨细胞瘤 (罕见瘤种), 特发性肺纤维化 (罕见病), 其他实体瘤
全新序列的CLDN18.2×CD47双抗,优秀的成药性、安全性和有效性
已完成支持IND的全部药学和非临床研究,计划2022 Q1向NMPA递交IND申请,2022 Q2向FDA递交IND申请
CLDN18.2/纳米融合Fc抗体
具有较强的ADCC效应,在体内多个模型中显示了良好的抗肿瘤效果
2022.01正式递交IND申报资料
创新型人源化单克隆抗体,靶点针对新型免疫检验点,对多个瘤种有一定疗效
联合其他IO药物可起到协同增效的作用
Fc工程优化设计,安全性更好


全人源IgG1抗PD-L1单克隆抗体,野生型Fc,有ADCC效应
临床 II 期单药治疗晚期非透明细胞肾癌临床正在进行中
临床 I 期单药治疗复发或转移性鼻咽癌正在进行中:安全性良好,初步有效性: ORR=26.7% (4/15)
BC003联合BC001用于治疗晚期实体瘤的Ia期临床试验正在进行
BC003多个联合用药的临床正在计划

重组抗EGFR人鼠嵌合型IgG1单克隆抗体, CDR区序列与西妥昔一致
Ia期单药以“3+3“方式完成了400、500、750mg/m2 3个剂量组爬坡,结果显示安全可耐受
Ib期临床联合化疗(TIP)治疗晚期阴茎癌:安全性可控,未观察到新的安全性信号; 初步有效性: ORR=94.1% (16/17); 关键性临床研究正在计划中
BC001联合BC003用于治疗晚期实体瘤的Ia期临床试验正在进行中

国内首个CSF-1R单抗
全人源IgG1单抗 ,具有ADCC功能
探索性临床 I 期正在进行中
进一步可开发的适应症包含:腱鞘巨细胞瘤 (罕见瘤种), 特发性肺纤维化 (罕见病), 其他实体瘤

全新序列的CLDN18.2×CD47双抗,优秀的成药性、安全性和有效性
已完成支持IND的全部药学和非临床研究,计划2022 Q1向NMPA递交IND申请,2022 Q2向FDA递交IND申请

CLDN18.2/纳米融合Fc抗体
具有较强的ADCC效应,在体内多个模型中显示了良好的抗肿瘤效果
2022.01正式递交IND申报资料

创新型人源化单克隆抗体,靶点针对新型免疫检验点,对多个瘤种有一定疗效
联合其他IO药物可起到协同增效的作用
Fc工程优化设计,安全性更好


